लेखक:
Mike Robinson
निर्मितीची तारीख:
7 सप्टेंबर 2021
अद्यतन तारीख:
11 मे 2024
सामग्री
अणु संख्या एखाद्या घटकाच्या एका अणूच्या मध्यवर्ती भागातील प्रोटॉनच्या संख्येशी संबंधित असते. हे मूल्य बदलत नाही; म्हणूनच, आपण न्युट्रॉनची संख्या यासारख्या समस्थानिकेची इतर वैशिष्ट्ये शोधण्यासाठी वापरू शकता.
पायर्या
भाग 1 चा 1: अणु संख्या शोधणे
नियतकालिक सारणीची एक प्रत शोधा. आपल्याकडे उपलब्ध नसल्यास येथे क्लिक करा. प्रत्येक घटकाची स्वतःची अणु संख्या असते; अशा प्रकारे, सामग्री शिकण्यासाठी कोणतेही शॉर्टकट नाहीत. सारणीची एक प्रत वापरा किंवा ती लक्षात ठेवण्याचा प्रयत्न करा.
- बर्याच रसायनशास्त्राच्या पुस्तकात मागील कव्हरवर टेबल छापलेले असते.

आपण सारणीमध्ये अभ्यास करीत असलेला घटक शोधा. बहुतेक सारण्यांमध्ये घटकांचे पूर्ण नाव आणि त्यांची चिन्हे समाविष्ट असतात (उदाहरणार्थ पारासाठी एचजी). आपण ज्याचा शोध घेत आहात ते आपल्याला न सापडल्यास, ऑनलाइन जा आणि "रासायनिक प्रतीक" या शब्दासह आणि त्या घटकाच्या नावाने शोध घ्या.
घटकाची अणु संख्या शोधा. हे सहसा घटकाच्या घराच्या वरच्या डाव्या किंवा उजव्या कोपर्यात असते परंतु ते इतर ठिकाणी देखील येऊ शकते. याव्यतिरिक्त, हे नेहमीच पूर्णांक मूल्य असते.- जर संख्येमध्ये दशांश बिंदूचा समावेश असेल तर ते कदाचित अणू वस्तुमान दर्शवेल.
जवळील घटकांनुसार माहितीची पुष्टी करा. नियतकालिक सारणी अणू संख्यांच्या क्रमानुसार आयोजित केली जाते. जर आपला आइसोटोप क्रमांक "33" असेल तर उदाहरणार्थ, डावीकडील घटक "32" असेल आणि उजवीकडे एक "34" असेल. त्या प्रकरणात, कारण आपण अणू क्रमांक पहात आहात.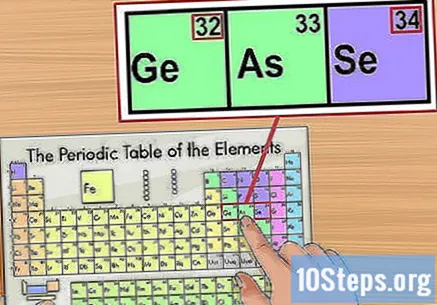
- "56" (बेरियम) आणि "88" (रेडिओ) घटकांमध्ये उडी आहे. या श्रेणीशी संबंधित आयसोटेप टेबलच्या खाली दोन ओळींमध्ये आहेत. ते फक्त अशाच प्रकारे विभक्त झाले आहेत जेणेकरून टेबल जास्त मोठे होणार नाही.
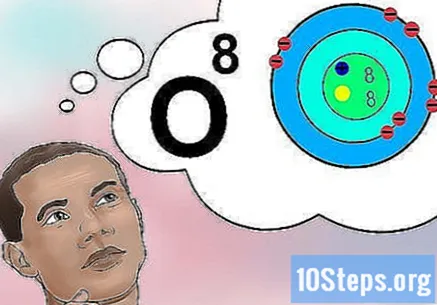
अणू संख्येचा अर्थ काय ते समजून घ्या. अणू संख्येची एक सोपी व्याख्या आहे: घटकाच्या अणूमधील प्रोटॉनची मात्रा. प्रोटॉनची ही मात्रा यामधून न्यूक्लियसचे एकूण विद्युत शुल्क निश्चित करते - जे अणू किती इलेक्ट्रॉन चार्ज करू शकते हे ठरवते. इलेक्ट्रॉन जवळजवळ सर्व रासायनिक संवादासाठी जबाबदार असल्याने, अणू संख्या अप्रत्यक्षपणे त्या घटकाच्या भौतिक आणि रासायनिक गुणधर्मांवर परिणाम करते.- दुस words्या शब्दांत, आठ प्रोटॉनसह प्रत्येक अणू ऑक्सिजन अणूशी संबंधित आहे. दोन ऑक्सिजन अणूंमध्ये न्यूट्रॉन किंवा (जर एखादा आयन असेल तर) किंवा इलेक्ट्रॉन असू शकतात परंतु त्यांचे प्रत्येकी आठ प्रोटॉन असतात.
भाग २ चा 2: अधिक महत्वाची माहिती शोधत आहे
अणूचे वजन निश्चित करा. हे सहसा नियतकालिक सारणीतील घटकांच्या नावाखाली येते आणि दोन किंवा तीन दशांश ठिकाणी असते. अणू वजन एखाद्या घटकाच्या अणूंच्या सरासरी वस्तुमानाशी संबंधित असते, ते निसर्गात कसे आढळते हे दर्शवते. हे "अणु द्रव्यमान युनिट्स" ("यू" किंवा "यू.एम.ए") मध्ये मोजले जाते.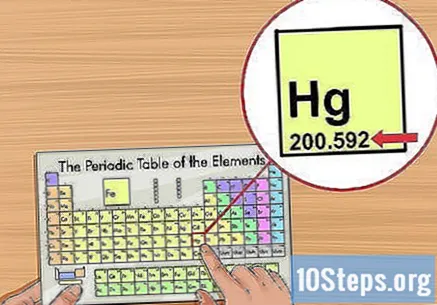
- बरेच शास्त्रज्ञ वजनाऐवजी "अणु द्रव्य" हा शब्द वापरण्यास प्राधान्य देतात.
अणू वस्तुमान समजून घ्या. अणू द्रव्यमानाची संकल्पना वजनाप्रमाणेच आहे. फरक असा आहे की वजन विशिष्ट घटकाच्या कोणत्याही अणूचा सरासरी वस्तुमान दर्शवितो, विशिष्ट अणूचा नाही. उदाहरणार्थ: एक ग्रॅम लोहामध्ये वेगवेगळ्या वस्तुमानांसह अनेक अणू असतात; वजन त्यांच्या "सापेक्ष वस्तुमान" दर्शवते. आपण घटकाच्या एका अणूचा अभ्यास केल्यास आपल्याला त्याचे विशिष्ट वस्तुमान माहित असणे आवश्यक आहे.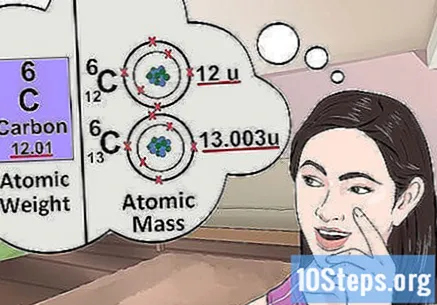
- सामान्यत: अणूंचा समावेश असलेल्या रसायनशास्त्राच्या समस्येमुळे आधीच अणू द्रव्यमानांची माहिती दिली जाते. जेव्हा आपल्याला एखादे भिन्न मूल्य दिसेल तेव्हा आपल्याला पहारेकरी न पकडण्याची संकल्पना समजून घेणे आवश्यक आहे.
वस्तुमान संख्येस गोल करा. घटकांची संख्या अणूमधील प्रोटॉन आणि न्यूट्रॉनच्या एकूण प्रमाणात असते. त्याची गणना करणे कठीण नाही: फक्त नियतकालिक टेबलवर मुद्रित अणू द्रव्य घ्या आणि त्यास जवळच्या संपूर्ण मूल्यापर्यंत गोल करा.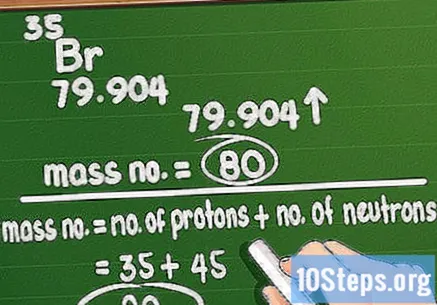
- हे कार्य करते कारण न्यूट्रॉन आणि प्रोटॉनचे प्रमाण 1 अमेरिकेच्या अगदी जवळ आहे, तर इलेक्ट्रॉनचे प्रमाण शून्याच्या अगदी जवळ आहे. अणु वस्तुमानात दशांश मूल्य निश्चित करण्यासाठी अचूक गणना असते, परंतु महत्वाची माहिती केवळ संपूर्ण संख्या असते जी आपल्याला सांगते की तेथे किती प्रोटॉन आणि न्यूट्रॉन आहेत.
- लक्षात ठेवा आपण अणू वस्तुमान वापरत असल्यास, आपण घटकातील विशिष्ट अणूच्या वजनाने गडबड कराल. उदाहरणार्थ, ब्रोमिनचा नमुना 79 or किंवा of१ चा अणु द्रव्य असतो.
न्यूट्रॉनची संख्या मोजा. आता आपणास आधीच माहिती आहे की अणु संख्या प्रोटॉनच्या संख्येइतकी असते आणि वस्तुमान संख्या प्रोटॉन आणि न्यूट्रॉनच्या संख्येच्या बेरजेइतकी असते. एखाद्या घटकामधील न्यूट्रॉनची मात्रा निश्चित करण्यासाठी, त्या संपूर्ण वस्तुमानापासून फक्त अणु संख्या वजा करा. काही उदाहरणे:
- हेलियम अणू (त्याच्या) ची संख्या 4 असते आणि अणू संख्या 2 असते. म्हणून, 4 - 2 = 2 न्यूट्रॉन.
- चांदीच्या नमुने (एजी) मध्ये सरासरी वस्तुमान संख्या 108 असते (नियतकालिक सारणीनुसार) आणि अणूची संख्या 47 असते. सरासरी प्रत्येक नमुन्यात 108 - 47 = असतात. 61 न्यूट्रॉन.
समस्थानिके समजून घ्या. समस्थानिक हा घटकांचा विशिष्ट प्रकार असतो, त्यात अनेक न्यूट्रॉन असतात. आपण ज्या समस्येचे निराकरण करू इच्छित आहात ते "बोरॉन -10" किंवा "बी" सारखे काहीतरी आणत आहे, कारण आपण 10 च्या मोठ्या संख्येसह बोरॉनच्या घटकांबद्दल बोलत आहात. हे मूल्य वापरा, "सामान्य" मूल्ये नव्हे बोरॉन च्या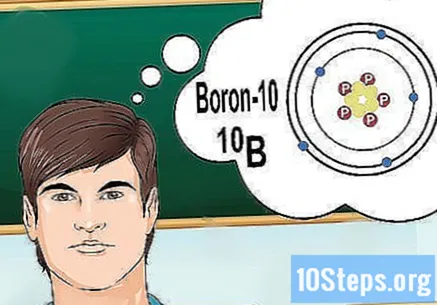
- समस्थानिकांची अणु संख्या कधीही बदलत नाही. घटकांच्या प्रत्येक समस्थानिकेमध्ये समान प्रोटॉन असतात.
टिपा
- काही जड घटकांचे अणू वजन कंसात किंवा चौरस कंसात येते. याचा अर्थ असा की हे वजन सर्वात समस्थानिकांचे सरासरी नसून सर्वात स्थिर समस्थानिकेचे अचूक द्रव्यमान आहे. शेवटी, याचा घटकांच्या अणु संख्यांवर परिणाम होत नाही.


